速收藏!患者如何入组干细胞临床试验,获得免费治疗的机会?
来源:九芝堂美科干细胞
2019-07-29
对于身患重病,传统治疗手段又无能为力的患者而言,入组临床试验,尝试新技术、新特药或许能重获生机。但是有些新药在国内还没有任何一个产品上市,患者很难找到入组信息。比如干细胞药品,虽然在国内还没有任何一个产品上市,但是它为很多找不到治疗方案的患者带来卓越疗效的临床案例却屡屡见诸报端。小美收集了相关信息,盘点了开展干细胞临床研究的医院和进行干细胞新药研发的企业,希望为想入组干细胞临床试验的患者指点一二。
2015年原国家卫计委和原食药监总局联合发文,明确了干细胞临床研究的备案制度,我国干细胞开始走向分别按药品、技术管理的“双轨制”道路。通常按照技术监管的称为干细胞临床研究,按照药品监管的称为干细胞临床试验。
要想寻找免费入组治疗的机会,就不得不先要了解一下干细胞管理的“双轨制”。
一、干细胞临床研究
哪些医院可以开展干细胞临床研究?
2015年7月原国家卫计委和国家食药监管总局联合发布的《干细胞临床研究管理办法(试行)》规定三甲医院需要完成“干细胞临床研究机构备案”和“干细胞临床研究项目备案”后才能开展临床研究,以下简称双备案。也就是说,只有完成机构备案的医院才能获得开展干细胞临床研究的资格,医院在完成机构备案的基础上完成项目备案才能真正开始研究,这是国家加强干细胞临床研究监管的具体措施。
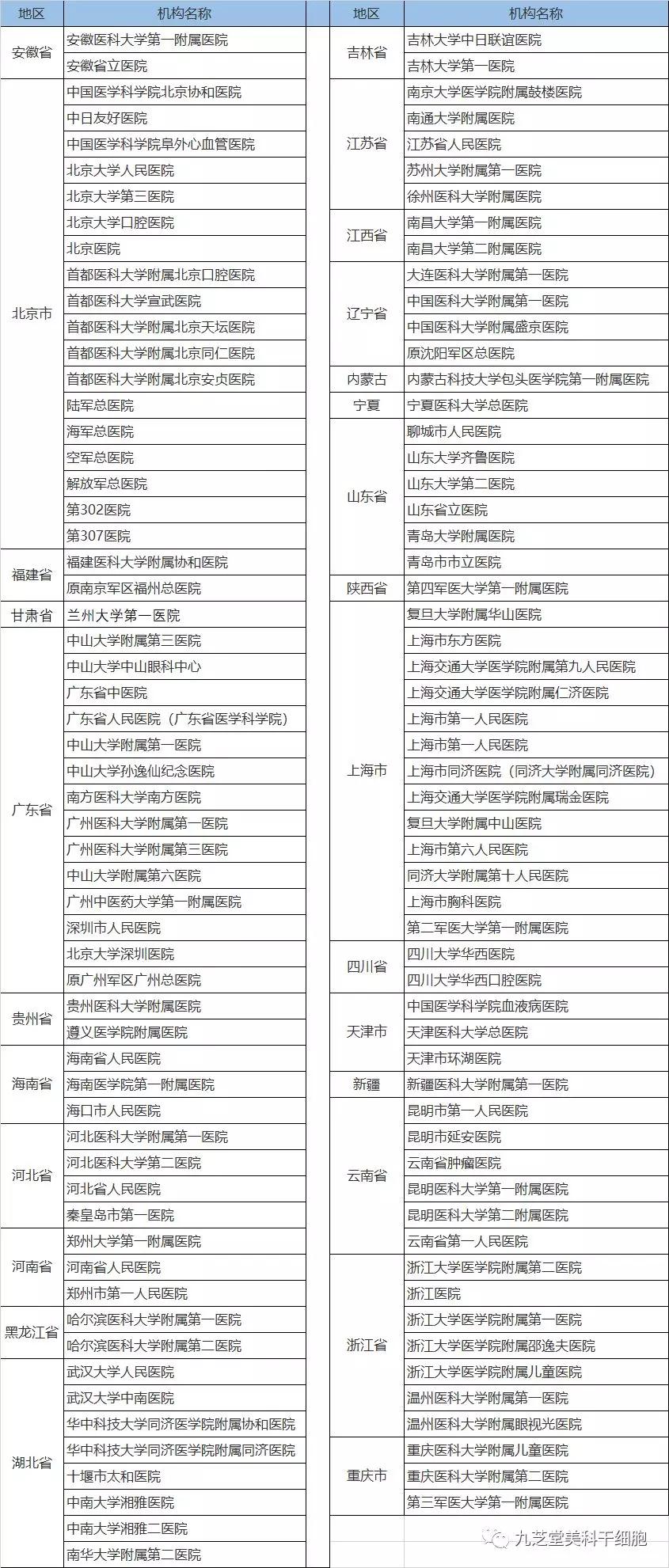
据南方日报报道,截至2019年6月,完成干细胞临床研究机构备案的地方医院增至104家,加上军队医院12家,备案的医院达到116家。国家对备案机构实施动态管理,今后会根据情况进行增加或减少。因此,入组临床研究一定要找完成备案的医院。
完成干细胞临床研究机构备案的医院
哪些疾病正在开展临床研究?
前面已经提到,仅仅完成了机构备案并不能开始干细胞临床研究,还需对要研究的具体研究课题进行备案。
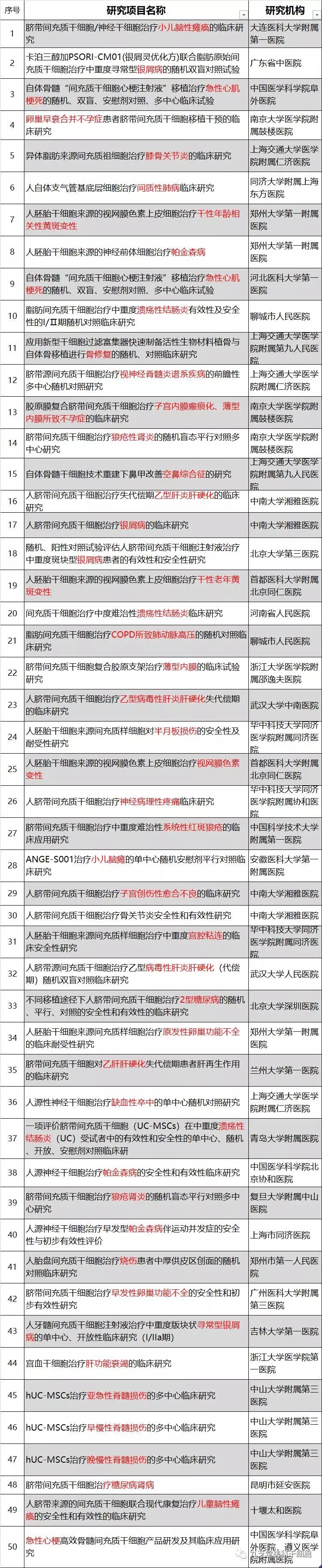
目前国内已经完成备案的干细胞临床研究有51项31种适应症,涉及妇科疾病、眼科疾病、消化系统、骨科疾病、神经系统疾病、心脑血管疾病、内分泌系统疾病、自身免疫性疾病等。
干细胞临床研究项目
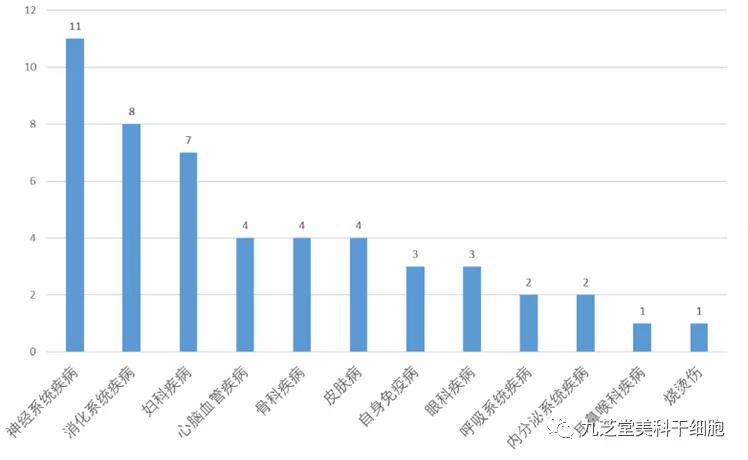
干细胞临床研究项目涉及疾病分类
116个研究机构目前只有51项研究完成备案,已经备案的干细胞临床研究机构到2020年底仍无研究项目备案的,需要重新提交机构备案材料,如果没有及时重新提交备案材料程序的视为自动放弃备案。因此可以预见将来还将陆续有更多的临床研究进行备案。
备案的临床研究项目使用的是什么细胞?
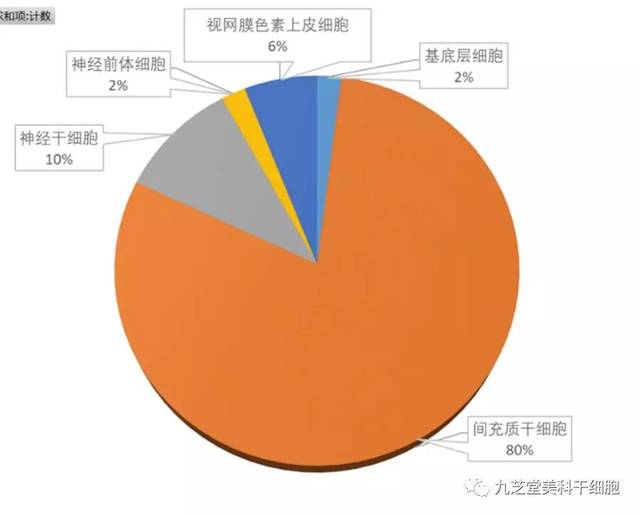
已备案的干细胞临床研究项目涉及多种细胞类型,包括间充质干细胞、神经干细胞、神经前体细胞、视网膜色素上皮细胞等,其中间充质干细胞是最常应用的一种干细胞,涉及研究项目40个,占比高达80%。
干细胞临床研究备案项目细胞类型统计
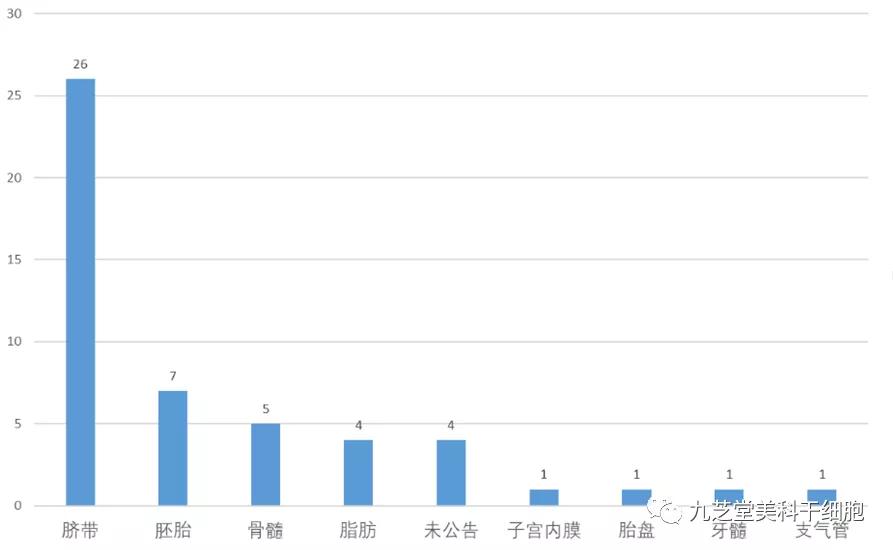
从组织来源看,脐带是最主要的组织来源,涉及研究项目26个,占比超过50%,胚胎、骨髓、脂肪也是常见组织来源,三项合计16项。
二、干细胞临床试验
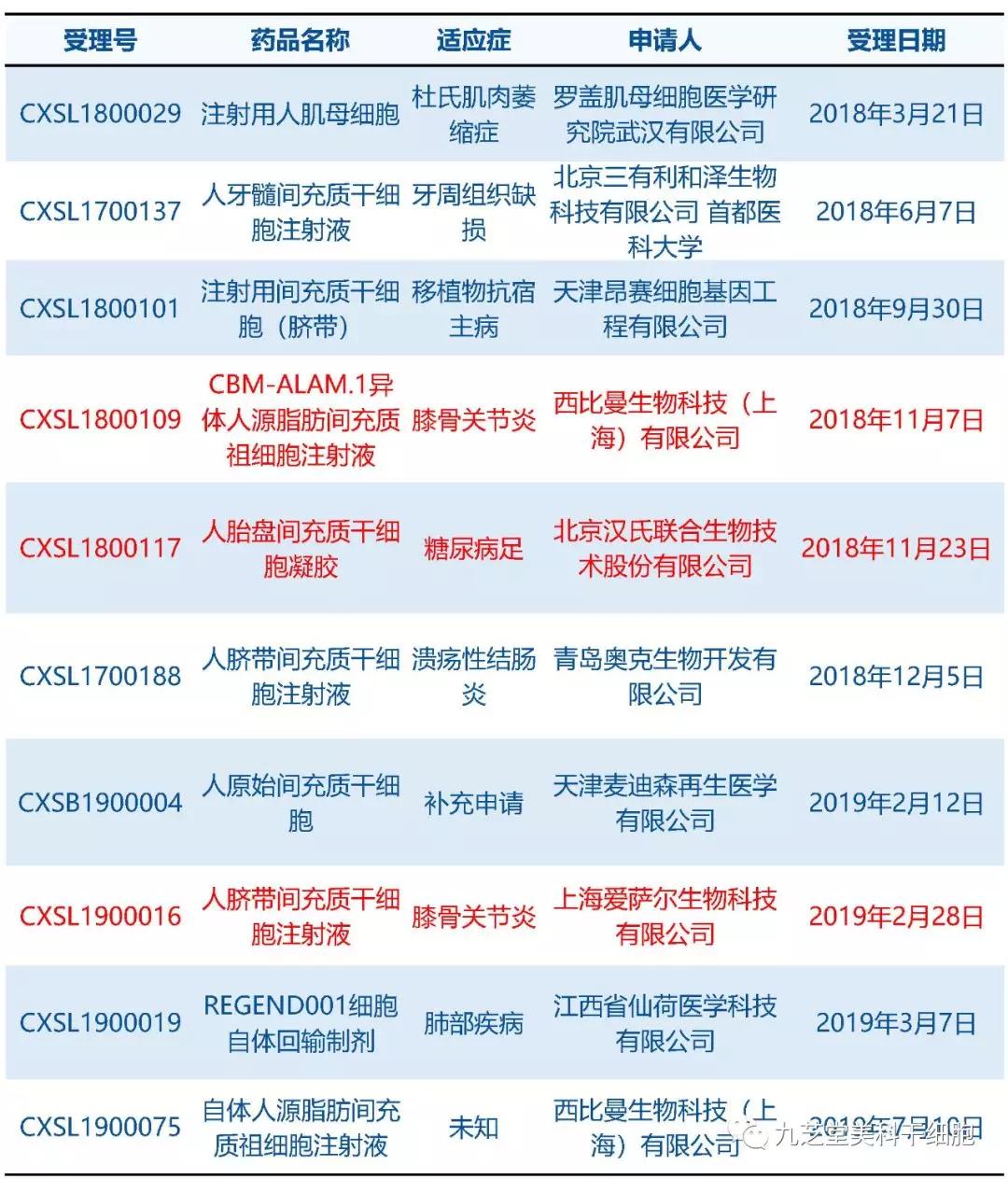
截至2019年7月18日,国家药品审评中心已经受理干细胞新药临床试验申请10项,其中3项已经获得许可进行临床试验,如下表所示,红字所示为已获准项目(不包含2018年以前已经过期的临床试验)。这些研究项由企业发起,如果想参与临床试验,可向企业直接咨询。
国家药品审评中心已经受理的干细胞新药临床试验
入组临床试验,需要具备什么条件?
临床试验通常会设定入组和排除标准。比如通过限制参与者的疾病种类、病情阶段,也可能对性别、症状和病史等做出要求,符合条件者才能够参与试验。
其次还要了解试验的目的是为了治愈疾病、减缓恶化,还是减少副作用?试验处于哪期阶段,是否符合你的需求?比如,第一期试验旨在确定安全的剂量,第三期试验旨在确定新疗法是否比旧疗法有效。明确你想要什么,然后看是否和该试验的目的吻合。
每一项临床试验的入选标准都有所不同,因此需要联系研究者或者通过临床研究公示网站获得信息,对照自身情况看看是否符合条件,不能确定的要咨询医生确定。
参与干细胞药品的临床研究一般设立的排除标准会包含以下几项(仅做示例):
1、 严重过敏体质;
2、 HBV/HCV/HIV/梅毒等感染筛查阳性;
3、 合并恶性肿瘤、造血系统疾病;
4、 妊娠期、哺乳期妇女;
5、 肝肾功能严重受损患者;
6、 过去5年内有精神障碍,药物/酒精滥用;或有精神病史并且目前尚未控制及药物疗效不稳定。
去哪找入组信息,如何联系?
可查询中国临床试验注册中心网站(www.chictr.org.cn)或药物临床试验登记和信息公示平台(www.chinadrugtrials.org.cn)获得已注册研究项目的信息,包括入组标准、排除标准、相关医疗机构的联系人信息等。未注册项目可直接联系医疗机构或药品研发公司获得信息。
上一条:
下一条: