一文读懂间充质干细胞治疗慢阻肺的原理
2021-06-21
人活一口气,可一旦患上慢阻肺,想畅快地吸一口气,比登天还难。想象一下,如果被活埋了,土已到嗓子眼的感觉;再想象一下,如果爬山时,嘴里有东西就像一口血一样卡在嗓子眼里的感觉,这些都是慢阻肺患者的真实感受。
慢阻肺(全称“慢性阻塞性肺疾病”,英文简称“COPD”)是呼吸系统疾病中的常见病和多发病,患病率和死亡率均高,主要症状为慢性咳嗽、咳痰、气急或呼吸困难、胸闷等。
世界卫生组织资料显示,全球约有2.1 亿 COPD 患者,每年有300 多万患者死亡。就我国情况而言,如果吸烟和空气污染状况不能得到有效控制,到2030年COPD 患者将达 300万之多[1]。另外随着中国人口老龄化,预计到2050年,中国60岁以上老年人口将达到4.98亿[2]。随着年龄的增加,肺纤维化、慢阻肺的发病率也将逐步上升,并且这些疾病的发生发展与衰老有着密不可分的联系,在衰老过程中的一些组织结构和分子表型变化可能参与了此过程[3]。
慢阻肺患者细胞衰老机制
根据以往研究来看,细胞衰老可通过至少两种非互斥的机制促成慢性阻塞性肺疾病。首先,在慢性阻塞性肺疾病中上皮细胞和内皮细胞凋亡增多,这造成了肺泡壁中细胞的损失,此时应该发生涉及细胞增殖的补偿机制,以消除肺泡细胞的丢失[4]。当细胞衰老发生时,其增殖能力丧失,平衡倾向于细胞凋亡并由此形成慢性阻塞性肺疾病。其次,有证据表明细胞衰老与炎症之间存在密切关系,衰老细胞可表现出NF-κB的活化,以及释放各种炎性细胞因子,导致炎症增强[5]。
这些与衰老相关的促炎机制在人肺组织中得到了证实,例如有研究发现在p16阳性的Ⅱ型肺泡上皮中,TNF-α表达量与对照组相比明显增加,并且这种p16阳性细胞的衰老程度与慢性阻塞性肺疾病炎症严重程度之间也存在着正相关性[6]。
另外,细胞衰老也被证明与特发性肺纤维化的发病密切相关。Hecker等[7]发现,老年肺纤维化小鼠模型的肺部存在着异于正常数量的衰老和抗凋亡的肌成纤维细胞,并且还证明了这些细胞在持续肺纤维化中起关键作用(见图1)。还有研究表明,支气管上皮衰老也是特发性肺纤维化进程的关键因素,其与患者支气管上皮的再上皮化密切相关,并且这种再上皮化可被SIRT6拮抗[8]。
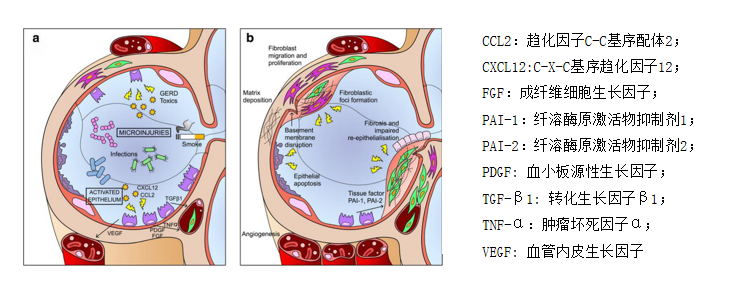
图1:IPF发病机制示意图。随着时间的反复损伤导致修复过程的不适应,其特点是AEC2s凋亡、增殖和上皮间质串扰(a)和随后的成纤维细胞、肌成纤维细胞增殖和细胞外基质的积累(b)。
衰老过程中也伴随着干细胞的衰老和耗竭,而这种干细胞耗竭现象对组织和器官的修复存在着严重不利影响,这也使得老年动物肺部在内外刺激的作用下更容易发生纤维化[9]。
慢阻肺的治疗瓶颈
目前对于肺纤维化、慢性阻塞性肺疾病(COPD)的治疗主要包括非药物管理(肺康复、补充氧气、手术治疗)和药物管理(糖皮质激素、免疫抑制剂、 支气管扩张剂和靶向药物)。但这些治疗方法也存在很多弊病,例如非药物管理中,患者很少能够按照要求进行肺康复训练,肺移植的来源和排斥反应都是很大的问题。在药物管理中,糖皮质激素和免疫抑制剂的应用会导致诸多并发症,且无法逆转已经存在的病变,支气管舒张剂的使用未被证实可以有效延长患者的生存期以及具有靶向药物局限性[10-11]。
大量理论与实践的研究证实:干细胞促进了再生医学的发展,在对抗重大疾病,颠覆药物治疗、手术治疗等传统医学模式具有不可估量的作用。同时,也为慢性阻塞性肺疾病患者带来了新的治疗方法。
间充质干细胞治疗慢阻肺
从目前已有的研究来看,间充质干细胞主要从5个方面对肺纤维化、慢性阻塞性肺疾病起作用。
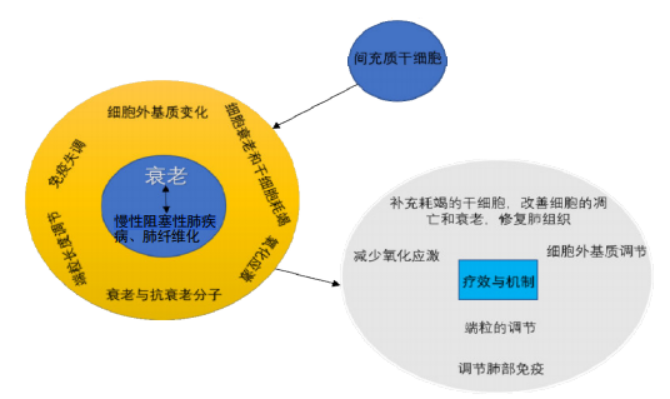
图2:间充质干细胞移植治疗慢性阻塞性肺疾病和肺纤维化的效果和机制。
端粒的调节:肺疾病伴随着端粒的改变,研究表明,特发性肺纤维化患者通过间充质干细胞治疗可减少其端粒的损耗,并改善患者的病情[12-13]。间充质干细胞可能通过减少肺泡上皮细胞、成纤维细胞等端粒的磨损,来延缓肺部疾病的进展,改善肺功能。
减少氧化应激:衰老过程中逐渐增强的氧化应激是导致肺疾病的重要因素。减轻氧化应激,可以改善肺组织的衰老、减少肺疾病的发生、延缓慢性肺病的进展。研究发现,间充质干细胞对组织的过度氧化应激有明显的改善作用。活性氧是细胞活动中消耗氧气而产生的物质,其与氧化应激密切相关。
Liu等[13]发现骨髓间充质干细胞可有效减少肺损伤大鼠肺组织中的活性氧,减轻肺部损伤。Huang等[14]研究发现骨髓间充质干细胞植入的肺纤维化小鼠模型肺组织中超氧化物歧化酶活性和总抗氧化活力显著增加,表明间充质干细胞可减轻肺组织氧化应激。另外,丙二醛和血红素氧合酶1是两种相拮抗的物质,前者具有增强氧化应激的作用,而后者则具有抗氧化应激和保护细胞的功能。Fredenblibgh等[15]发现间充质干细胞可在降低肺部丙二醛水平的同时增加血红素氧合酶1的合成。
补充耗竭的干细胞,调节相关分子,改善细胞凋亡和衰老,修复肺组织:间充质干细胞可作为已耗竭干细胞的一种补充,通过抗凋亡的作用,治疗肺纤维化、慢性阻塞性肺疾病。目前,已有报道称骨髓间充质干细胞在体内外都可分化为肺泡上皮细胞,且能在肺部定植。例如Huang等[16]发现通过静脉植入骨髓间充质干细胞能减轻肺纤维化大鼠肺纤维化的程度,并且能定植在模型大鼠肺部,分化为Ⅱ型肺泡上皮。Liu等[17]发现,植入小鼠肺损伤模型的人脐带间充质干细胞能发挥抑制细胞衰老和凋亡的作用,肺组织中有间充质干细胞定植。另外,间充质干细胞还可在特定部位分泌各种因子来抑制衰退,修复肺组织,见图3。
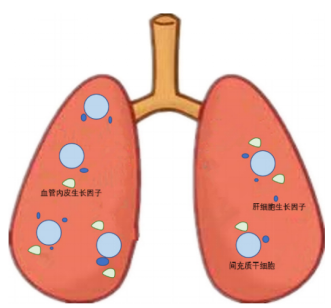
图3:间充质干细胞在肺部分泌细胞因子。间充质干细胞在肺部分泌肝生长因子和血管内皮生长因子, 促进肺部损伤的修复。
调节肺部免疫:肺疾病与机体免疫力下降、免疫调节失衡密切相关。间充质干细胞的低免疫原性和免疫调节作用已经得到公认[18]。Gupta等[19]证明间充质干细胞移植能降低慢性阻塞性肺疾病小鼠肺泡灌洗液炎症因子TNF-α水平,上调抗炎因子IL-10水平,并且可有效改善内毒素造成的肺损伤。同样,Li等[20]也报道了间充质干细胞对肺纤维化小鼠肺部炎症有明显的抑制作用,并且可以改善其纤维化程度。Jackson等[21]发现间充质干细胞可通过隧道纳米管样结构将自身的线粒体转移到巨噬细胞内,从而调节巨噬细胞的功能,使其吞噬细菌的能力增强,见图4。
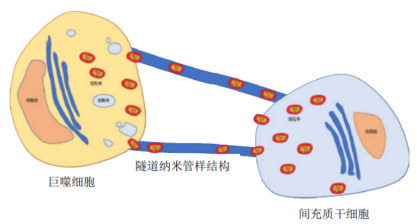
图4:间充质干细胞通过隧道纳米管样结构向巨噬细胞转移线粒体。
调节细胞外基质:在肺疾病中,细胞外基质发生明显改变。现已有多项研究表明间充质干细胞可作为调节细胞,改善细胞外基质的病理性改变。Moodley等[22]在因博来霉素而产生肺纤维化的小鼠中,胶原蛋白沉积可以通过间充质干细胞的调节而改变。同时,Fikry等[23]在经间充质干细胞治疗的大鼠肺纤维化模型中找到胶原蛋白沉积减少的证据。另外,间充质干细胞也可通过降低胰蛋白酶的活性,逆转基质金属蛋白酶9、基质金属蛋白酶12的表达从而调节慢性阻塞性肺疾病模型中肺部细胞外基质的变化、减轻肺气肿病变、改善其肺功能[24]。
低氧,让骨髓间充质干细胞能力更强
间充质干细胞不仅具有自我更新和分化能力,而且能够在衰老损伤部位分泌多种具有生物活性的因子(如神经生长因子、血管内皮生长因子、血管内皮生长因子受体2、碱性成纤维生长因子等)、与其他细胞相接触传导信号、将自身具有良好功能的结构转移到受损细胞(如线粒体的转移)等方式,起到免疫调节、抗凋亡、血管生成、促进局部干/祖细胞的生长和分化等作用。因此间充质干细胞可能是治疗与衰老相关的慢性阻塞性肺疾病、肺纤维化的有效手段[25]。
九芝堂美科的美国合作方Stemedica公司在其位于加洲的cGMP设施中开发了临床级别的细胞生产平台BioSmartTM ,该平台模拟细胞在人体内的微环境,在连续低氧条件下生产的缺血耐受人骨髓间充质干细胞(it-hMSC)能力更强,在治疗慢性阻塞性肺疾病中发挥的作用会更大。
目前,已有越来越多的临床研究探讨了干细胞治疗慢性阻塞性肺疾病的安全性和有效性,并且取得了很大的突破。相信有一天,干细胞治疗慢性阻塞性肺疾病将会取得更大的进展,为更多患者缓解疾病痛苦和改善生活质量。
未来,九芝堂美科将不断加大对干细胞领域的研发力度,促进成果转化及应用,造福人类健康。
上一条:




