87版红楼梦贾蓉饰演者杨俊勇离世,给我们提了什么醒?
2021-11-19
近日,87版《红楼梦》贾蓉饰演者杨俊勇心脏病突发去世,享年57岁。杨俊勇的突然离开让人惋惜,但也给人们敲响了警钟,秋冬季是心血管疾病的高发时节,尤其要警惕急性心梗的发生。

近年来,随着我国经济的迅速发展、生活方式的转变以及人口老龄化的加剧,急性心肌梗死(AMI)的发病率和死亡率呈逐年增长趋势,心血管病成为我国疾病死因第一位 [1]。根据马尔科夫模型预测,未来20年间中国将新增2100万急性冠脉事件,发生700万例心源性死亡 [2]。2001~2011十年间,中国因ST段抬高型心肌梗死(STEMI)住院患者人数翻了两番,从3.50/10万人增长到15.40/10万人 [3]。且AMI死亡率呈现快速增长趋势,从2002~2015年,农村地区AMI死亡率从12.00/10万人升至70.09/10万人,城市地区从16.46/10万人升至56.38/10万人 [4]。
心肌梗死有救吗?
急性心肌梗死 (acute myocardial infarction,AMI )是危害人类健康的重大疾病,在发达国家被称为“头号杀手”,是世界范围的主要死亡原因。
利用传统手段治疗心肌梗死患者时,医生的首要治疗原则就是开通为心脏供血的冠状动脉,尽快恢复心肌的血液再灌注,主要手段包括溶栓和介入治疗。溶栓就是使用药物消融血栓,恢复血液通畅,使用溶栓治疗血管通畅率达到50%~70%,然而服用大量药物后会带来一系列副作用;介入是通过手术去除血栓,给堵塞的血管手术安装支架,将血管撑开,让血液流畅,但手术价格高、副作用大。严重者可以进行心脏移植,但又存在器官短缺以及免疫排斥等问题,无法广泛发展。
由此可见,药物、介入和心脏移植术等治疗方法,虽然可以部分改善心肌缺血,但都无法从根本上挽救梗死的心肌。
炎症是造成心梗后不良后果的罪魁祸首
目前对心梗的紧急救治已经卓有成效,但仍无法控制进展性的左室不良重构 [5]。究其原因发现,心梗发生后的促炎性免疫反应对心肌愈合是一把双刃剑(如图1所示),适度的促炎反应利于从伤口中清除死细胞并促进心肌修复;而过度的炎症级联反应的激活会刺激一系列细胞反应(如图2所示),可能会延长损伤并导致心室的不良重塑 [6-9]。因此,过度的免疫/炎症反应可能是这些患者渐进性心肌功能障碍的重要原因。
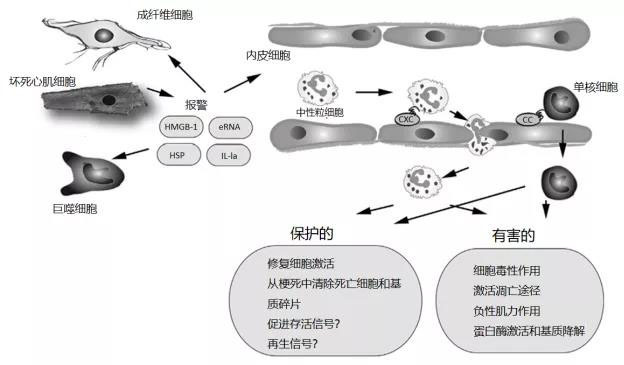
图1. 梗死后的炎症反应对梗死心脏既有保护作用,也有有害作用。坏死的心肌细胞会释放危险信号,激活先天免疫反应,从而诱导细胞因子和趋化因子。CXC 和 CC 趋化因子与内皮表面的糖胺聚糖结合,介导梗死区域中性粒细胞和单核细胞的募集。浸润的白细胞对梗死的心脏产生广泛的保护作用和有害作用。有人提出浸润的中性粒细胞可能会延长缺血性损伤,对心肌细胞产生细胞毒性和促凋亡作用。此外,白细胞衍生的分泌产物可能具有负性肌力作用,并且蛋白酶可能增加基质降解,导致梗塞心脏的不良重建。白细胞可能具有的保护作用表现在其亚群可以吞噬死细胞和基质碎片,并可以通过激活内皮细胞和成纤维细胞来促进修复。最近的研究表明,髓系细胞的亚群也可能对心肌细胞产生促存活和再生作用。eRNA,细胞外RNA;HMGB-1,高度保守的NNA结合蛋白;HSP,热休克蛋白,热休克蛋白:IL-la,白细胞介素la。
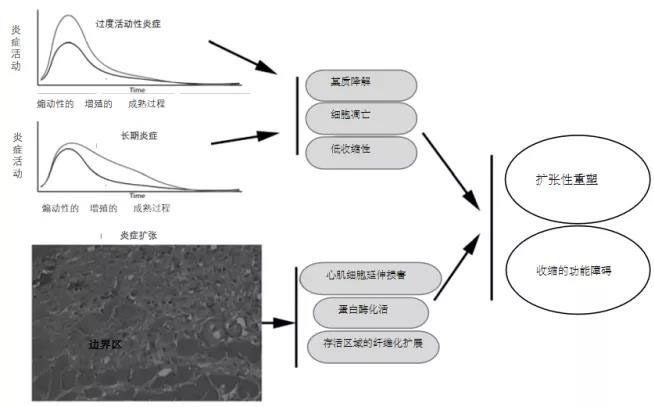
图2. 过度、延长和扩大的炎症反应的后果是梗塞后心脏的不良重构。过度活跃或长期炎症可能通过刺激蛋白酶活化而加剧基质降解。细胞因子表达增加可能会增加心肌细胞凋亡并抑制收缩力。梗死后炎症反应的空间抑制缺陷可能导致可存活心肌区域炎症损伤的扩大,从而导致纤维化的扩大。梗塞后炎症的负调节受损可能导致不利的扩张重塑并加剧收缩功能障碍。
这一发现提示了科研工作者——找到一种物质/方法,它能够调控梗死后炎症的细胞效应和分子信号的表达,遏制住心脏的不良重构和进行性的心功能障碍。
间充质干细胞治疗心脏炎症,改善心脏功能
2017年,Stemedica公司在国际知名学术杂志Circulation Research上发表了题为《Systemic Anti-Inflammatory Effects Improve Left Ventricular Dysfunction in Acute Myocardial Infarction and Ischemic Cardiomyopathy》[10]一文,文中的研究结果表明静脉注射间充质干细胞(MSC)用于急性心肌梗塞可减轻大面积梗死小鼠的左室功能进行性恶化和不良重塑,在缺血性心肌病中,它们可以改善左室功能,其作用原理部分是由全身抗炎作用来实现的。
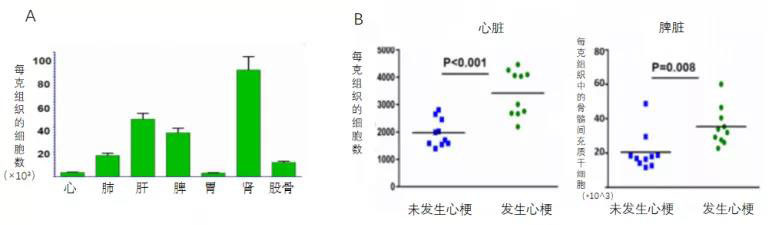
首先,在过去大家都认为干细胞移植到受损心肌后,最终的功能修复是依赖于外源性干细胞的直接替代和刺激内源性心肌细胞的再生,但是在本项研究中,研究者发现在小鼠AMI后24小时,通过心脏左前降支静脉注射的MSC经荧光标记追踪显示,在小鼠肝脏、脾脏和肾脏中有高浓度的细胞,仅有一小部分间充质干细胞移植到了心脏(图3A)。与未发生心肌梗死的动物的心脏相比,AMI小鼠脾脏中MSC的积累显著增加(图3B),表明AMI产生了全身抗炎信号,导致脾脏MSC的归巢和积累。
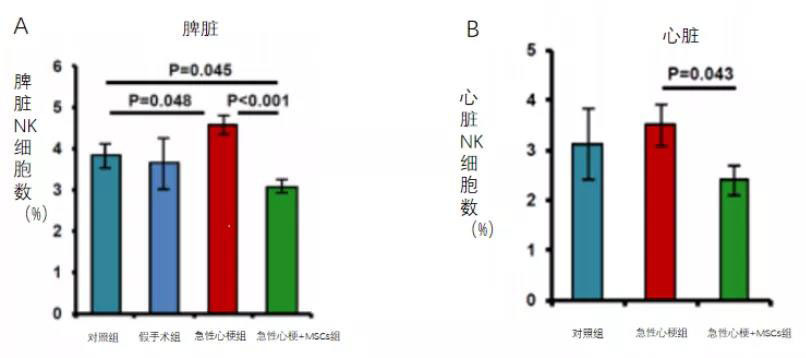
其次,研究者对心肌梗死后第7天的大鼠静脉注射人源性间充质干细胞后发现,AMI后7天小鼠脾脏NK细胞显著增加,MSC显著诱导了脾脏中NK细胞的减少(图4A)。同样在心脏中也观察到了MSC诱导的NK细胞减少(图3B)。
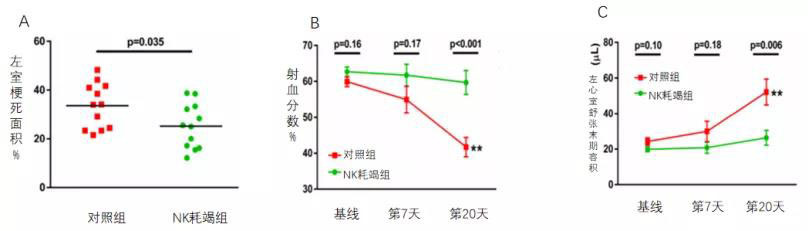
那么,心肌中NK细胞的减少是否直接影响了心脏功能的改善呢?研究者在接下来的实验中发现: 在AMI前24小时接受抗NK1.1抗体介导的NK细胞耗竭的小鼠中,MI后20天的梗塞面积明显较小(图5A);AMI前NK细胞的耗竭显著减弱了AMI后心功能的恶化;与对照组相比,NK耗竭组的梗死面积明显缩小(图5A),射血分数显著升高(图5B),左室舒张末期容积显著降低(图5C)。
更为有趣的是,在对小梗塞与大梗塞小鼠治疗结果的比对结果中发现:MSC治疗可改善不良的左室重塑,且这些影响对于MIs≥LV的25%(中度梗死面积为25%)的小鼠更为显著。在该亚组中,MSC治疗阻止了对照组表现出的舒张末期容积的统计学显著增加(图6B),并且有防止LVEF降低的趋势(图6A)。
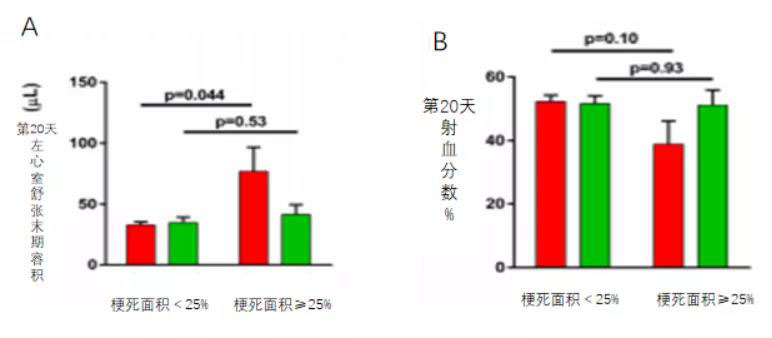
图6A. 在对小梗塞与大梗塞小鼠治疗结果的比对结果中发现:MSC治疗可改善不良的左室重塑,且这些影响对于MIs≥LV的25%(中度梗死面积为25%)的小鼠更为显著。MSC治疗阻止了对照组表现出的舒张末期容积的显著增加。
图6B. 在对小梗塞与大梗塞小鼠治疗结果的比对结果中发现:MSC治疗可改善不良的左室重塑,且这些影响对于MIs≥LV的25%(中度梗死面积为25%)的小鼠更为显著。MSC治疗阻止了对照组表现出的有效防止LVEF降低的趋势。
Stemecida的研究给医学界对于心肌梗塞的治疗带来了新的启迪,静脉注射间充质干细胞(MSC)后,间充质可以自动归巢于心肌、脾脏、肾脏等组织,并通过降低局部心肌炎症、全身炎症反应而改善心肌功能及不良的左室重构。静脉注射间充质干细胞治疗急性心肌梗塞有希望成为一种实用而安全、有效的临床治疗策略。
参考文献:
[1] MoranA,GuD,ZhaoD, .FuturecardiovasculardiseaseinChina:Markovmodel and risk factor scenario projections from the coronary heartdiseasepolicymodel China[J].CircCardiovascQualOutcomes, 2010,3(3):243 252.
[2] Li J,Li X,Wang Q,et al. ST-segment elevation myocardial infarction in China from 2001 to 2011 (the China PEACE-Retrospective Acute Myocardial Infarction Study): a retrospective analysis of hospital data[J]. The Lancet,2015,385(9966):441-51.
[3] 陈伟伟,高润霖,刘力生,等. 《中国心血管病报告2017》概要[J]. 中国循环杂志,2018,33(1):1-8.
[4] O′Gara PT,Kushner FG,Ascheim DD, .2013 ACCF/AHA guide- line fo rthe management of ST elevation myocardial infarction:are- port of the American College of Cardiology Foundation/American Heart AssociationTask Forceon Practice Guidelines[J].Circulation,2013,127(4):362 425.
[5] Westman PC, Lipinski MJ, Luger D, Waksman R, Bonow RO, Wu E, Epstein SE. Inflammation as a driver of adverse left ventricular remodel- ing after acute myocardial infarction. J Am Coll Cardiol. 2016;67:2050–2060. doi: 10.1016/j.jacc.2016.01.073.
[6] Reinecke H, Minami E, Zhu WZ, Laflamme MA. Cardiogenic differentiation and transdifferentiation of progenitor cells. Circ Res. 2008; 103:1058–1071. [PubMed: 18988903]
[7] Entman ML, Youker K, Shoji T, et al. Neutrophil induced oxidative injury of cardiac myocytes. A compartmented system requiring CD11b/CD18-ICAM-1 adherence. J Clin Invest. 1992; 90:1335–1345. [PubMed: 1357003]
[8] Christia P, Frangogiannis NG. Targeting inflammatory pathways in myocardial infarction. Eur J Clin Invest. 2013; 43:986–995. [PubMed: 23772948]
[9] Faxon DP, Gibbons RJ, Chronos NA, Gurbel PA, Sheehan F. The effect of blockade of the CD11/ CD18 integrin receptor on infarct size in patients with acute myocardial infarction treated with direct angioplasty: the results of the HALT-MI study. J Am Coll Cardiol. 2002; 40:1199–1204. [PubMed: 12383565]
[10] Systemic Anti-Inflammatory Effects Improve Left Ventricular Dysfunction in Acute Myocardial Infarction and Ischemic Cardiomyopathy




