全国爱眼日:关注视网膜黄斑变性的干细胞治疗
2020-06-08
明眸皓齿、炯炯有神、顾盼神飞、神采飞扬、 目光如炬……都是用来形容眼睛的美丽的词汇。但是眼睛的各种损伤和退化几乎无法治疗,视网膜退行性疾病是现代社会造成视力损伤的主要发病原因,给患者造成明显的生活质量下降。
人口老龄化与黄斑变性
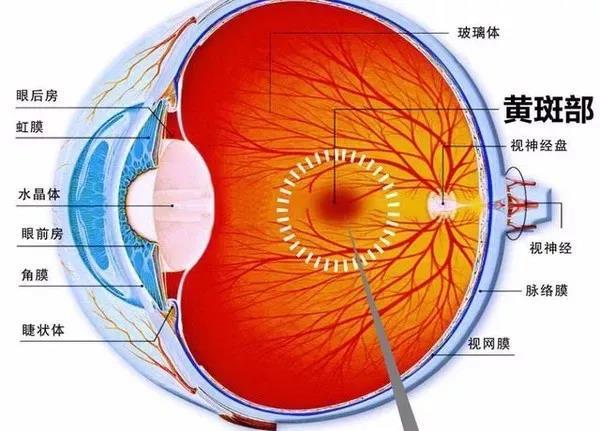
黄斑变性(AMD)是视网膜退行性疾病之一,由于视网膜细胞数量的进行性减少,主要包括视网膜色素上皮细胞和光感受器细胞的不可逆损失并最终导致视觉功能丧失,是眼部致残的重要原因。人类从外界所获取的信息90%以上来自于视觉系统,失去光明与身患癌症一样令人类蒙受极大的恐慌与打击。
AMD多发生于50岁以上人群,双眼先后或同时发病,其中一只眼发病者,另一只眼5年内发病率为40%。在美国,黄斑变性导致的失明比青光眼、白内障和糖尿性视网膜病变这三种常见病致盲人数总和还要多。在日本,近年来50岁以上年龄群的黄斑变形发病率达到1%,呈现急速上升趋势,总人数约在70万人,被列为疑难疾病之一。在中国,黄斑变性发病率更高,60-69岁发病率为6.04%-11.19%。随着中国人口老龄化,该病有明显的上升趋势。
老年性黄斑变性(AMD)在全球范围影响了超过3000万人的生活。
干细胞治疗黄斑变性前景广阔
目前临床上用来治疗黄斑变性的药物和方法非常有限,多以抗炎治疗及神经细胞营养保护性药物延缓病程,或使用抑制血管生长类药物,但现有药物治疗无法恢复已经受损的视神经细胞和功能视网膜色素上皮(RPE)细胞。
利用干细胞可以替代或修复受损视神经细胞和RPE细胞,前景广阔。研究显示,将干细胞衍生的视网膜色素上皮(RPE)移植到视网膜下,结果显示细胞不仅能存活和改善视觉功能,还能长期保护视锥和视杆细胞。
美国FDA已批准多种细胞类型用于临床治疗退行性眼病的Ⅰ/Ⅱ期临床试验,如图所示:
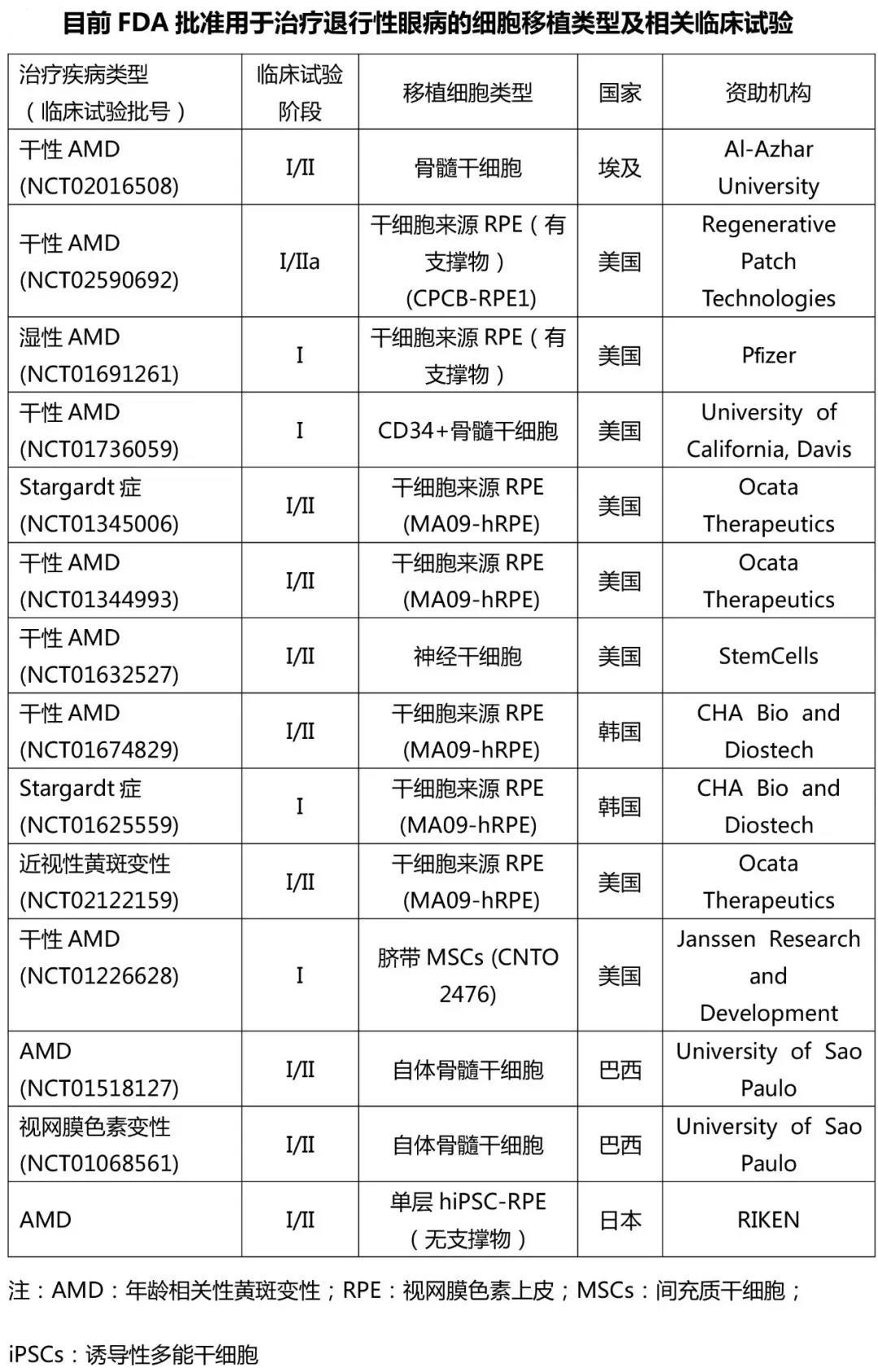
干细胞治疗一切安全和良好疗效的前提是制备合格的干细胞。制备不合格的细胞,反而会引发新的疾病。这是需要非常严谨和严肃对待的问题。
新药品法明确规定干细胞治疗产品按药品管理
2019年新药品法明确将药物分为中药、化药和生物制品三个类别,干细胞属于生物制品类别下的细胞治疗产品,将按照药品管理,2020出台细胞治疗产品的GMP附录。
按照国家监管要求,目前用于疾病治疗的干细胞需为经当地药监或卫生部门批准使用的干细胞产品,原则上应在GMP条件下生产,并严格按照药品相关规定做好质量控制。
GMP是一套适用于制药、食品等行业的强制性标准,要求企业从原料、人员、设施设备、生产过程、包装运输、质量控制等方面按国家有关法规达到卫生质量要求,形成一套可操作的作业规范帮助企业改善企业卫生环境,及时发现生产过程中存在的问题,控制风险。
三十多年来的实践证明,GMP确实是一套行之有效的先进的科学管理制度,特别对消灭药品生产过程中的污染、混淆和差错的隐患,保证药品质量起到重要的作用。
九芝堂美科——中国干细胞制药的先行者
2018年,九芝堂参与发起设立的珠海横琴九芝堂雍和启航基金(以下简称雍和启航基金)投资了美国Stemedica细胞技术有限公司,同时投资成立了九芝堂美科(北京)细胞技术有限公司,作为Stemedica干细胞技术在中国的唯一承接方。
Stemedica公司拥有15年干细胞研发生产经验, 2010年获得了美国加利福尼亚州政府颁发的生产许可证,至今已经在GMP条件下运行了近10年时间。
Stemedica公司在全程低氧条件下生产的缺血耐受人骨髓间充质干细胞(ithMSC)产品,其生产工艺和质量体系符合美国FDA cGMP 要求。
目前九芝堂美科已完成技术转移,并在中国药谷——北京大兴生物医药基地建成了符合中国、美国cGMP标准质量体系的生产平台,可生产符合中、美药品申报要求的临床级干细胞。




